CULTIVO HIDROPONICO COMO HERRAMIENTA DE PROPAGACIÓN, CULTIVO DE PLANTAS MADRES Y MEDIO PARA EL ENRAIZAMIENTO DE ESQUEJES
Por: Marta Ines Hurtado
Gómez
PROHOSA S.A. Mayo
27 de 2001
mhurtado@multi.net.co
Bogotá D.C., Colombia
S.A.
Probablemente, la civilización se inició cuando el hombre antiguo aprendió a sembrar y a cultivar ciertas clases de plantas para su satisfacción. A medida que se fue haciendo necesario incrementar la cantidad de plantas útiles, especies y variedades se empezó a mejorar en las técnicas de la propagación de las plantas. La mayor parte de las plantas cultivadas se perderían o revertirían a formas menos deseables a menos que se propaguen técnicamente y bajo las condiciones requeridas por cada especie.
Una de estas técnicas consiste en la introducción de los cultivos hidropónicos o cultivados en sustrato, es decir, un medio diferente al suelo. Se podría plantear que en la floricultura Colombiana, las áreas destinadas a la propagación de plantas, son pioneras en el desarrollo y establecimiento de estos sistemas.
De acuerdo con lo citado por H.M. Resh, en la selección de la ubicación más adecuada para el establecimiento de los cultivos hidropónicos, se debe tener en cuenta:
La exposición solar lo más directa posible al este, sur y oeste, con cortavientos al norte, superficie nivelada o que pueda ser fácilmente nivelada; buen drenaje interno, con un mínimo de precolación de una pulgada por hora; existencia de energía, bien sea gas natural o corriente trifásica, teléfono y agua de muy buena calidad y cantidad, al menos, de galón y medio por planta / día; cerca de la residencia para facilitar la vigilancia de los invernaderos durante las condiciones climáticas extremas; orientación Norte - Sur de los invernaderos con cultivos en línea de la misma orientación; una región que tenga la máxima cantidad de radiación solar; evitar sitios que tengan vientos excesivamente fuertes.
Tecnológicamente es posible el control activo de todos los parámetros requeridos en la propagación de plantas y semilleros. Sin embargo en los cultivos ya establecidos se hace necesario adecuarlos para lograr minimizar los riesgos de tipo ambiental como temperatura e intercambio del CO 2 mediante la construcción de ventanas con apertura cenital y lateral logrando un efecto chimenea especialmente significativo y llegar así a una superficie de apertura óptima del 32 % de la superficie cultivada. La ubicación de las ventanas deberá estar sujeta a un estudio de clima del invernadero y su ambiente externo; estudio que comprende temperatura, vientos y humedad relativa.
En las plantas madres de clavel, es vital que el intercambio gaseoso se realice y que la temperatura no suba de 28 º C, pues se afecta la cosecha al tornarse flácidos los esquejes por pérdida de turgencia. Si los paquetes con esquejes ingresan al cuarto frío con temperaturas altas, superiores a 10 ºC, pueden escaldarse, es decir se pierde el material. Si no es posible contar con una infraestructura de ambiente controlado, será necesaria la implementación de cortinas y demás recursos que estén al alcance para que con un programa de cierre y apertura se pueda controlar, caso específico en heladas por ejemplo, la temperatura al interior del invernadero en la noche no debe bajar de 3 ºC y en el día no debe subir de 28ºC. A menudo es difícil controlar estos rangos solo con el manejo de las cortinas, entonces se puede hacer uso de microaspersión que ayuda a bajar un poco la temperatura, aunque no siempre la turgencia.
Las condiciones de clima en los bancos de enraizamiento difieren de las de la planta madre, pues en el invernadero es importante que la humedad relativa sea alta. El delta térmico entre el día y la noche no debe ser muy alto. El rango óptimo depende de la especie cultivada; rangos entre 10ºC y 27ºC y temperaturas del sustrato de 21 – 22 ºC, para miniclavel puede ser adecuado. Se debe tener presente que también en esta área se requiere el intercambio gaseoso, por lo tanto se debe contar con cortinas que faciliten este requerimiento. En los primeros días de siembra, es importante tener bastante cuidado con el manejo de estas pues, corrientes de aire muy fuertes puede deshidratar el esqueje así se esté cumpliendo con los requerimientos hídricos. En los días del endurecimiento, la apertura de las cortinas debe ser más frecuente y sin descuidar la nebulización de mantenimiento.
Hay diversos medios y mezclas que se usan en las operaciones de propagación, tales como germinación de semillas, enraizado de estacas y esquejes y cultivo de plantas madres o plantas en maceta.
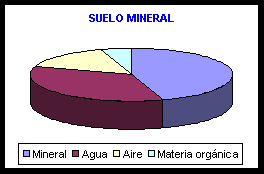
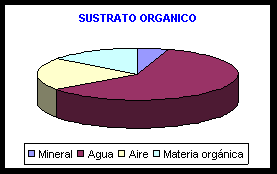
De acuerdo con Ansorena Miner, el suelo mineral es el medio de cultivo universal para el crecimiento vegetal, aunque en las plantas cultivadas en maceta o contenedor ha sido progresivamente sustituido por sustratos con proporción mayoritaria de componentes orgánicos.
Normalmente se denomina maceta a un recipiente de corta duración, mientras que se reserva el nombre de contenedor para designar los recipientes en que la planta va a permanecer durante largo tiempo. En términos prácticos, llamaré contenedor al recipiente en que se aloja el sustrato y se produce el desarrollo de la planta.
Además de servir de soporte o anclaje a la planta, el medio de cultivo tiene que suministrar a las raíces unas cantidades equilibradas de aire, agua y nutrienes minerales. Si las proporciones de estos componentes no son adecuadas, el crecimiento de la plantas podrá verse afectado por asfixia, deshidratación, exceso o carencia de nutrientes, enfermedades producidas indirectamente por los anteriores.
La proporción de la fase sólida del sustrato respecto al suelo (consecuencia de su elevada porosidad), lo que indica que en un volumen determinado de sustrato habrá mas espacio disponible para el agua y el aire que en el mismo volumen de suelo. Esto explica que las plantas puedan desarrollarse en volúmenes de sustrato tan reducidos como los contenidos en una maceta, a causa de sus mejores propiedades físicas.
Las proporciones de las fases sólida, líquida y gaseosa en un medio de cultivo varían con la naturaleza del medio y con las condiciones exteriores (drenaje, temperatura, humedad, etc).
|
|
|
Ansorena Miner, Javier. Comparación de la composición de un suelo mineral y un sustrato organico
Dentro de la fracción sólida del suelo la mayor parte es mineral, mientras que en los sustratos orgánicos suele predominar la materia orgánica. Esta podrá estar más o menos descompuesta, lo que también influirá en sus propiedades.
La elección del medio se deberá determinar por el costo, calidad y el tipo de método de cultivo hidropónico seleccionado El medio no debe contener ningún tipo de material tóxico. La grava y arena de origen calcáreo se deben evitar, pues pasan al medio gran cantidad de carbonato de calcio generando un incremento en el pH.
El medio deberá ser suficientemente duro para poder durar bastante tiempo. Los agregados muy blandos deben evitarse ya que pierden muy rápido su estructura y el tamaño de sus partículas va disminuyendo, lo cual trae como resultado una compactación que produce una pobre aireación de las raíces; sustratos como la escoria presentan esta característica como también la de tener bordes muy agudos situación que puede romper raíces o cuello de la planta cuando hay movimiento de ella por viento o manejo abriendo la puerta de entrada a muchos microorganismos. Si es necesario emplear este tipo de sustrato, se recomienda que los primeros 5 cms de la superficie de este medio sea de otro sustrato más "suave", de forma que se prevenga cualquier lesión que la planta pueda recibir.
Ansorena, opina que consecuencia del ataque de los micoorganismos, la materia orgánica se descompone y experimenta una serie de cambios en su composición, hasta que alcanza una cierta estabilidad biológica. Estos cambios habrán de tenerse en cuenta en los sustratos basados en sustancias orgánicas naturales, como la turba, las cortezas y otras de diversos orígenes.
En el caso de las turbas, al tratarse de materiales que han estado sometidos durante largo tiempo a los procesos naturales de degradación biológica, su estabilidad es elevada y no existe riesgo de descomposición.
Otros materiales como la corteza de pino y la mayoría de subproductos y residuos orgánicos, han de sufrir la descomposición microbiana antes de su empleo como sustratos, según el proceso que se conoce como compostaje. Si este no es adecuado se producirán fenómenos fitotóxicos y de inmovilización de nitrógeno.
El diseño depende de la especie y forma a cultivar. Para plantas en maceta es recomendable el sistema con gotero individual, el cual se inserta en el sustrato cerca de la zona radicular. La descarga de estos goteros varía de acuerdo al requerimiento tanto de la planta como del sustrato. En bancos donde se siembran las plantas sin maceta, el sistema a emplear puede ser de líneas de goteo. Dependiendo del sustrato y de las condiciones climáticas y los requerimientos de la planta se tomará la decisión de cuantas líneas por banco y a que distancia deben de estar los goteros, los cuales pueden estar a 10, 20 ó 30 cms, pero siempre conservando la misma distancia entre ellos pues es necesario para el control del volumen del fertiriego.
En bancos de enraizamiento, el sistema preferiblemente debe ser aquel que genere niebla de gota muy fina. Existen nebulizadores con gotero individual o de 4 nebulizadores, es decir en forma de cruz. Lo más importante es que se logre una nebulización que cubra bien el follaje y no genere demasiado drenaje a nivel de follaje y de banco. Si con el sistema elegido se generan gotas de gran tamaño, se pueden presentar situaciones como que, por más riego que se suministre, el esqueje se deshidrate, o haya pérdida de agua o excedentes de agua en el sustrato. La distancia entre nebulizadores estará dada por el traslape de la nube al llegar a la superficie del banco, de tal manera que se eviten los parches de deshidratación. La nebulización debe tener un sistema de control y homogenización de la presión para obtener el resultado esperado.
El sistema general de riego debe contar con los filtros necesarios para evitar que los goteros tanto de plantas madres como de enraizamiento se taponen.
Plantas Madres:
El banco o recipiente donde se cultiven las plantas madres debe ser preferiblemente libre de poros para permitir una correcta desinfestación una vez finalizado el ciclo. Sin embargo, es común encontrar bancos de concreto o fibrit que soportan directamente el sustrato o bolsas de polietileno o macetas que contienen el sustrato. Conociendo el contenedor se debe procurar una excelente desinfestación y contar con un muy buen sistema de drenaje. En la madera las colonias de hogos pueden sobrevivir por varios años
Con el fin de evitar posible pérdida de plantas sembradas en el contenedor seleccionado, es necesario que a este se le programen mantenimientos preventivos ya que, en el caso del fibrit o del concreto tienden a "pandearse" por el peso del sustrato y dilatación del hierro interno por la temperatura del vapor.
Las plantas madres cultivadas en matera, tienen las ventaja con respecto a las que están sembradas en banco corrido que al estar individualmente, se pueden eliminar fácilmente cuando hay presencia de alguna enfermedad que la afecte y evitar así la contaminación o ruptura de raíces de las vecinas. También se facilita el drenaje vertical en la matera y aireación, generando plantas con mayor cantidad de pelos absorbentes y por ende mejor calidad.
Bancos de enraizamiento:
Emplear bandejas como soporte del sustrato elegido trae ventajas como el de formar "plug", el cuál facilita la siembra en sitio definitivo y evita el maltrato de las raíces. Además, dependiendo de la bandeja elegida, se puede incrementar la densidad de siembra.
El suelo puede contener semillas de malezas, nemátodos y ciertos hongos y bacterias nocivas para las plantas. El fenómeno llamado ahogamiento, que es muy común en plantas madres o bancos de enraizamiento, es causado por hongos del suelo como Pythium, Rhizoctonia, además de otras enfermedades como las causadas por Fusarium sp, y Alternaria sp. Para evitar la presencia de estos organismos es necesario tratar el sustrato preferiblemente con vapor. Para evitar la recontaminación del sustrato, es indispensable emplear plantas no infectadas y tratar las semillas con funguicidas. Los bancos o contenedores, el invernadero y todos los elementos que se requieran para el proceso de enraizamiento o de las plantas madres deben ser igualmente desinfectados; en general, se debe disponer de una asepsia general y profunda.
Según Hartman y Kester, el calentamiento de mezclas de suelo ricas en estiércol, tierra de hoja o compost, acelera la descomposición de la materia orgánica, en especial si ya está parcialmente descompuesta. Esto conduce a la formación de compuestos tóxicos para las plantas, haciéndose necesario lavar con agua limpia y retardar la siembra o transplante de 3 a 6 semana- Los materiales no descompuestos, como las turbas no resultan muy afectadas con el tratamiento de calor.
Temperaturas superiores a 85 ºC, también descompone algunos compuestos químicos complejos del suelo, produciendo cantidades crecientes de sales solubles de nitrógeno, manganeso , fósforo, potasio y otros. Algunas de éstas, particularmente el nitrógeno en forma amoniacal, pueden encontrarse en las primeras semanas que siguen al tratamiento con vapor en cantidades tales que pueden ser tóxicas a las plantas. Después, el amoníaco es convertido a nitrógeno nítrico, el cual alcanza su máximo en unas 6 semanas. La presencia del superfosfato en las mezclas de suelo inmoviliza el manganeso excesivo que se libera con el calentamiento impidiendo daños por toxicidad del mismo.
Para el tratamiento de sustratos el vapor es la mejor fuente de calor y la de empleo más común. La tubería debe estar colocada entre 15 y 20 cms debajo de la superficie. Al calentar el sustrato que debe estar húmedo pero no mojado, la recomendación estándar ha sido de una temperatura de 90ºC durante 1 hora. Algunos autores recomiendan una temperatura menor par evitar la muerte de algunos organismo benéficos que puedan estar presentes en un sustrato orgánico y para evitar problemas de toxicidad.
En la desinfestación con vapor es importante tener en cuenta los siguientes aspectos: (Cheever David)
Para la reutilización del sustrato, es importante monitorear los niveles de pH y sales y dependiendo de sus niveles se deben hacer lavados profundos con agua libre de sales. Los niveles de amonio y manganeso pueden subir con la aplicación del vapor. (Hartman y Kester)
El éxito que se obtiene en el bloque madre y en enraizamiento depende en gran medida de la selección del sustrato, de su preparación y de su desinfestación o asepsia inicial.
Sustratos como la turba, tanto para la siembra de plantas madres como en bancos de enraizamiento no requieren desinfestación, debido a su origen. Al coco por el contrario se le han detectado poblaciones muy altas de algunas especies de fusarium, alternaria y bacterias. Otros sustratos como las cascarillas de arroz, quemada y sin quemar también deben ser desinfectadas con vapor para evitar poblaciones de malezas y de collembolos y simfilidos.
Cuando la escoria es reciclada, previo a la desinfestación requiere ser tamizada para eliminar un porcentaje del polvo que se va produciendo por su descomposición natural. Si el banco no cuenta con suficiente drenaje y hay excedente de polvo de escoria , la probabilidad de que se taponen los macro poros y el mismo orificio de drenaje es muy alta. Normalmente cuando existe gran cantidad de este polvo, al final del ciclo se detectan zonas muy compactas en el banco y por ende, las raíces son delgadas, oscuras y con pocos pelos absorbentes. Plantas sembradas en otros sustratos como turba, coco, cascarillas no presentan este comportamiento. Tanto sistema aéreo como radicular se pueden desarrollar óptimamente, siempre y cuando se maneje de una manera muy conciente el fertiriego y su frecuencia teniendo en cuenta el comportamiento del clima y la edad de la planta.
Plantas sembradas en fibra de coco.
Proviene de la molienda en seco del mesocarpio de la nuez de coco, principalmente de Sri Lanka, India y Filipinas. Se importa en bloques compactados. Antes de su empleo se debe hidratar con lo que alcanza a expandir su volumen aproximadamente 3.5 veces su tamaño, (Dato por comprobar ya que en la realidad se encuentran bloques que expanden solo 2 veces su tamaño) teniendo una relación de 1 ton compactada 12 m3 de sustrato. Para cumplir con este requerimiento, se hace necesario introducir los bloques en tanques o tinas con agua, dejar allí algún tiempo hasta que se complete su hidratación y expansión total. (Plantaflor 1999)
Contiene sales ricas en fósforo y potasio, que provienen de la alimentación natural de la palma en zonas próximas al mar. Es decir, las sales son naturales y particularmente el potasio y sodio en forma de cloruro es el que eleva la conductividad en rangos de 2.5 a 3.5 mmhos/cm3 , usando en método de extracción con agua destilada. Estas sales son fácilmente lavadas con un riego intenso que se debe hacer antes de sembrar y verificar que el agua drenada salga completamente cristalina. Antes de ser empleado el sustrato es necesario dar un suplemento de Magnesio y Calcio. (Plantaflor, 1999)
Al ser un material orgánico pasa por un proceso de descomposición lento debido a su alto contenido de lignina (45.5%), con lo cual se logra mantener una relación Agua y oxígeno óptimo sobre un mayor período. El sustrato tiene una vida aproximada de 8 a 10 años, sin embargo si se efectúa un cambio del cultivo relacionado con la vida útil comercial de la planta ( 3 a 6 años promedio) se recomienda cambiar también la fibra de coco, el cuál podrá ser utilizado como materia orgánica para el suelo. En plantas madres o cultivos semestrales es factible reutilizarlo, no sin antes realizar un análisis químico de micro y macroelementos y hacer nuevamente la desinfestación. (Plantaflor, 1999)
El contenido de espacio aéreo (20%), genera un desarrollo radicular más intensivo, con marcada presencia de pelos absorbentes. Teniendo en cuenta su origen y recolección, es un material que requiere ser desinfectado para ser empleado en bancos de enraizamiento y en plantas madres. Se detectan microorganismos como Fusarium roseum, F. avenaceum, Botrytis, Alternaria, entre otros. También es común encontrar semillas de malezas.
Sí no se cuenta con un adecuado sistema de drenaje, ojalá vertical, se pueden acumular nutrientes y sales, lo que irá en contravía de la calidad de las plantas allí sembradas. Para lograr un adecuado balance entre la nutrición y la cantidad de riego proporcionado al cultivo, se hace indispensable que se cuente con un sistema donde se pueda calibrar exactamente el volumen a aplicar por banco o matera, de lo contrario se genera desuniformidad no solo en la acumulación de nutrientes sino en el desarrollo mismo de las plantas.
Si la fibra de coco no queda bien lavada, o si durante el ciclo del cultivo no hay un control del fertiriego y del drenaje, se puede acumular Sodio. He relacionado altos contenidos de sodio con tallos que se tuercen y entrenudos rajados en plantas de 1 mes de establecidas. De ahí la importancia del lavado que se realice.
Excedentes de agua en el sustrato generan la formación de algas , musgo y líquenes que restringen en cierta medida su oxigenación y facilita la proliferación de insectos plagas como es el caso del Fungus gnat, medio adecuado para su crecimiento e incremento de poblaciones.
Cuando se preparan sustratos orgánicos a partir de sustancias naturales, es necesario tener en cuenta las valores de la relación C/N; cuanto más bajo sea el valor de este cociente, más mineralizado estará el material.
Plantas sembradas en escoria o con mezclas
En la floricultura Colombiana, la escoria ha sido uno de los sustratos más empleados en la propagación de plantas, tanto en plantas madres como en enraizamiento, probablemente debido a la gran disponibilidad que hubo durante algunos años. Sin embargo, en la medida que se investiga en otras opciones se puede concluir que puede ser reemplazada sin mayores inconvenientes siempre y cuando el cambio se realice paulatinamente, es decir cuando se conozca el manejo apropiado del nuevo sustrato.
En bancos no muy profundos, es decir unos 15 cms, y con deficiencias en el sistema de drenaje, se hace indispensable que en cada ciclo se retire la escoria del banco y se zarandee con el fin de retirar y/o conocer el tamaño de partícula presente.
Con la homogeneidad de la granulometría es importante tener cuidado pues, si quedan macroporos muy grandes, las raíces pierden contacto con el sustrato ocasionando deshidratación, desbalance nutricional y por ende lixiviado de fertilizante. Para mi ha sido importante conocer cual es la participación porcentual de los diferentes tamaños de las partículas, pues busco un equilibrio que no genere compactación o exceso de macroporos. Esto se logra tamizando la escoria, en nuestro caso utilizamos una zaranda circular, de manera que el polvo se separe de las partículas de 2 – 6 mm (fina); una vez separado cada grupo, se procede a hacer una mezcla con una cantidad conocida de polvo y de escoria fina. También se obtienen buenos resultados también mezclando la escoria fina con cascarilla de arroz quemada; con estas mezclas se busca, entonces contar con la porosidad y retención ideal que debe tener un sustrato.
Mezclas de escoria fina y turba dan excelentes resultados ya que la turba almacena agua que en algún momento la planta va a necesitar y se aprovecha la ventaja de la escoria en cuanto al drenaje se refiere. Se puede presentar un inconveniente al reciclar esta mezcla, pues si estamos partiendo del principio que la escoria se "meteoriza", va a ser necesario retirar el sustrato del banco una vez finalice el ciclo y al tamizar se podría eliminar algo de la turba o se altera la participación de cada uno de los sustratos que de la mezcla.
Antes de iniciar un ciclo de siembras de plantas madres es recomendable conocer a través de un análisis de macro y micronutrientes los contenidos de la escoria y con este hacer los ajustes necesarios a la fórmula de fertilización. Es importante tener en cuenta que puede tener altos contenidos de elementos menores, especialmente Zinc.
Plantas sembradas en turba ( Mezcla de peat most, perlita y / o vermiculita)
En mi opinión, es el sustrato que mayores ventajas presenta, debido a todas sus características tanto físicas como químicas. Comercialmente se consigue con el pH corregido y con una adición de nutrientes que varía de acuerdo a los requerimientos. Una vez finalizado el ciclo, no es necesario retirar la turba, solo basta con la desinfestación después de retirado el material vegetal; este procedimiento hace más económica la labor por el ahorro de mano de obra. Debido a su baja descomposición es un sustrato que puede durar varios ciclos, lo único que requiere es que se adicione una pequeña capa de turba como reposición de la que se llevaron las raíces anteriores.
Antes de realizar la siembra se debe partir de un análisis de laboratorio y conocer la capacidad de intercambio catiónico. Es importante tener en cuenta que las cargas eléctricas de la superficie de las partículas de turba están en grupos compactos, lo que significa que grandes cantidades de nutrientes pueden ser retenidas en la disolución interna. El objetivo de la fertilización debe ser el manejo de estos almacenamientos de nutrientes de tal forma que, entre ellos, estén en las proporciones adecuadas.
En sustratos orgánicos como fibra de coco y turba, se recomienda que antes de la siembra se realice una incorporación de Trichoderma para evitar que hongos fitopatógenos como el fusarium sean los que primero colonicen. En este tipo de sustratos este antagonista coloniza perfectamente, con énfasis en la turba, medio apropiado para su establecimiento.
Bancos de enraizamiento
Las condiciones climáticas de los bancos destinados al enraizamiento del material de propagación asexual, están enfocadas a minimizar la pérdida de humedad relativa del ambiente para evitar la deshidratación del material. Es común encontrar que en los bancos la temperatura el delta térmico sea alto, generando estrés en el material. Lo ideal, es que durante el día la temperatura no exceda los 27 ºC y que en la noche no baje de 10ºC. Se debe evitar una temperatura del aire demasiado alta, debido a que tiende a estimular el desarrollo de yemas con anticipación al desarrollo de las raíces, y a incrementar la pérdida de agua por las hojas.
La temperatura puede regular la producción de raíces. Sí no se cuenta con las condiciones apropiadas de temperatura en el sustrato se puede aplicar artificialmente calor debajo del banco, para mantener en la base de las estacas una temperatura superior a la que se tiene en las yemas, induciendo así la iniciación de las raíces antes que se estimulen las yemas. Temperaturas homogéneas de 21 º C en la base de los esquejes produce mejor enraizamiento que temperaturas que fluctúan ampliamente. Sin Embargo, bajo las condiciones de la Sabana de Bogotá, se puede obtener un óptimo enraizamiento con diferentes sustratos así la temperatura del sustrato no sea homogénea durante el día.
En el siguiente gráfico se observa un promedio de lecturas de temperaturas tomadas a los sustratos a diferentes horas del día.
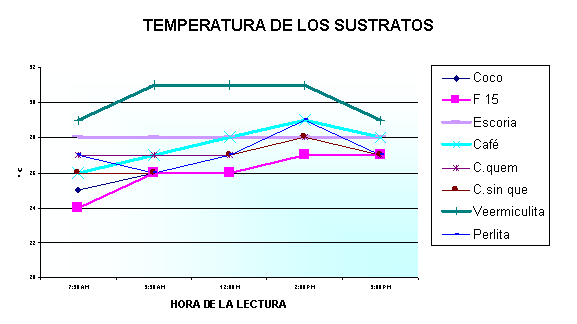
La selección del sustrato para enraizar, depende de varios factores, entre ellos la disponibilidad de agua y de equipo de nebulización, ya que dependiendo de estos factores y del manejo, es decir tiempos y frecuencias de riego van a depender los resultados. Para el caso del la turba o F 15, hay una reducción significativa en el volumen de agua a aplicar con énfasis a partir de la segunda semana de siembra, esto debido, a la retención de humedad que tiene. Para su manejo hay que tener en cuenta lo anterior y entrenar al personal de riego de bancos a que programe el controlador de riego a las condiciones de sustrato, clima y edad del esqueje, Una situación similar se presenta con la fibra de coco, debido a la gran capacidad de retención de agua que tiene. En el caso de los sustratos como cascarillas, (arroz y café), perlita y escoria en donde la retención es menor, se debe contar con una mayor disponibilidad de agua. Es recomendable que en bancos de enraizamiento se realice una aplicación de Trichoderma sp, con el fin de que el esqueje vaya protegido desde este sitio a campo con este antagonista.
En general, la frecuencia y duración del riego, depende del clima, de la edad del esqueje en enraizamiento y del sustrato. No es prudente hacer una recomendación de tiempos de riego a menos que el controlador de riego cuente con un sensor de humedad y temperatura.
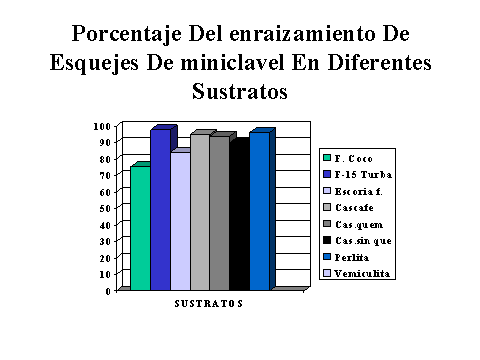
En términos generales, es factible enraizar en los sustratos anteriormente mencionados con resultados favorables en cuanto a la generación de raíces propiamente dicha, sin embargo, es vital conocer cual va a ser el comportamiento del esqueje en establecimiento pues si viene de enraizamiento con un sustrato que no retenga humedad o que no aporte nutrientes, la planta se puede ver afectada ante un error en campo. De ahí la importancia en enraizar en sustratos que protejan el sistema radicular, no se caiga y además le aporten a la planta agua y nutrientes, caso turba.
En el siguiente gráfico se observa el porcentaje de enraizamiento obtenido con diferentes sustratos:
Hormonas de enraizamiento
Las plantas cuentan con acumulación de hormonas de enraizamiento como auxinas. Dependiendo de la forma como se almacenen los esquejes la concentración de esta aumentará ó disminuirá. Hacer un pre-tratamiento a los esquejes colocándolos con las bases hacia arriba durante varios dias a 8 – 1º ºC, estimula la formación de primordios radiculares y reduce el tiempo de nebulización hasta en 1 semana (Cheever, 2000)
Sí durante el período de almacenamiento de los esquejes estos se ubican en la caja con las bases hacia arriba o acostados la probabilidad de que se concentre la auxina en la base es mayor. Esta situación favorece un enraizamiento natural, es decir, sin aplicación extra de hormonas. Sin embargo, desde el punto de vista práctico no todas las variedades cuentan con la misma concentración, por tal motivo es recomendable para asegurarse de que se va a obtener un enraizamiento homogéneo se asperje la base de los esquejes con una solución de AIB y ANA.
Siembra del material vegetal para enraizamiento
En este proceso no solo es importante que el material vegetal genere el sistema radicular como tal, sino que este sea protegido de rupturas que se puede traducir en pérdida del mismo o ser puerta de entrada para patógenos como diferentes especies de Fusarium.
Con el fin de mejorar la eficiencia y evitar la situación anteriormente descrita, es recomendable que el material de propagación se siembre en bandejas, para las cuales existe en el mercado máquinas que las llenan con el sustrato. En el caso de semillas, se cuenta con las totalmente automatizadas que a su vez las siembran y se trasladan por medio de bandas transportadoras. Hay bandejas que cuentan con bases que la separan del cemento o del piso, favoreciendo con esta circulación de aire en la zona radicular el "spin out", fenómeno fisiológico donde se regula el crecimiento y proliferación de raíces de una manera natural o inducida.
Al cosechar o arrancar los esquejes sembrados en "banco corrido", es decir sin bandeja o contenedor se corre el riesgo de que la situación anteriormente descrita ocurra. Para evitar tal situación se cuenta en el mercado con bandejas de diferentes tamaños y capacidad de alvéolos. Es factible que estas bandejas se llenen con el sustrato elegido, sin embargo no todos pueden formar plug, el cuál facilita la siembra una vez sea extraído del contenedor y a su vez protege la raíz. Sustratos como la turba y el coco forman fácilmente el plug, en cambio en los inorgánicos este tiende a desintegrarse, desprotegiendo las raíces y por ende la perdida de la ventaja inicial del plug.
Calidad y cantidad de agua aplicar en la propagación de plantas, son requisitos extremadamente importantes a tener en cuenta.
Plantas madres
Cantidad: En la práctica los cultivadores aplican una cantidad estimada de agua de acuerdo al sustrato empleado y al contenedor (longitud, ancho y profundo) por un tiempo específico. Para el cálculo se toma en cuenta el diseño del equipo de riego empleado, el sustrato, los requerimientos de la planta y las condiciones climáticas.
Cuando se está diseñando el sistema de riego se debe tener en cuenta las características físico-químicas del sustrato y sus requerimientos, las características del contenedor (banco), el drenaje, los requerimientos de la planta, las condiciones climáticas como vientos, temperatura y humedad relativa; con esta información se diseñará para que el sistema permita dar varios impulsos de riego al día.
En las plantas madres sembradas en "banco corrido" es común encontrar sistema de riego por goteo en el cuál los goteros se ubican a una distancia homogénea a lo largo del banco y esta puede variar entre 20 y 30 cms. Lo importante es que exista el traslape de bulbos, situación que varía de acuerdo al sustrato. Otro sistema de siembra es plantas individuales en maceta o bolsa plástica, para lo cuál se inserta un gotero en ella. Este sistema tiene la ventaja en el aseguramiento de que la nutrición se está dando a cada planta y es relativamente sencillo identificar cual gotero se encuentra taponado. Sin embargo, al no existir traslape de bulbo, se corre el riesgo de una mayor deshidratación de la planta por no recibir riego de otros goteros.
Para plantas madres de clavel, es recomendable que se den dos o tres impulsos al día, decisión que depende de la temperatura, vientos y humedad relativa. Si se permite que las plantas se deshidraten se dificultará la cosecha lo que repercute no solo en el daño fisiológico a las plantas, sino al daño en la calidad de los esquejes y la pérdida de rendimientos y tiempos de cosecha por no ser prudente cosecharlas cuando las plantas no están túrgidas ya que, si son cosechados al llegar al cuarto frío o de empaque ya están deshidratados. De manera que el volumen de riego promedio para bancos corridos que tengan 4 líneas de gotero a cada 30 cms es de 98 lts/ banco, 2.78 litros/ m2 / riego .
Para evitar la acumulación de sales en el sustrato, se recomienda que una vez a la semana se aplique solo agua, de manera que sirva de lavado. En sustratos como coco o escoria con "polvo" el lavado es difícil cuando no se cuenta con una sistema adecuado de drenaje en el banco. He ensayado diferentes modalidades para drenar estos medios en los bancos existentes. La mejor alternativa es ser muy precisos en la aplicación de la formula de fertilización, volumen y frecuencia de riego.
La demanda de agua se incrementa dramáticamente en los meses de verano por la evaporación, situación que está ligada a la temperatura ya la humedad relativa.
CALIDAD DEL AGUA
El agua para riego debe ser testada periódicamente para determinar su calidad. La concentración de nutrientes presentes como el hierro justifica ser tenidos en cuenta para el balance de la fórmula de riego. El agua también puede contener elementos perjudiciales o microorganismos para lo cual se requiere un tratamiento correctivo.
La tabla siguiente lista algunos de los más importantes factores considerados en la calidad del agua para riego de plantas sembradas en plugs o en sustrato.
|
FACTOR |
LIMITE SUPERIOR PARA PROPAGACIÓN EN SUSTRATO |
|
Factores de pH |
|
|
PH |
5.4 a 6.3 |
|
Alcalinidad |
100 ppm CaCo3 ( 2 meq/lt) |
|
Carbonatos totales TC |
100 ppm CaCo3 ( 2 meq/lt)100 |
|
Bicarbonatos (HCO3) |
122 ppm (2 meq/l) |
|
Dureza ( Ca+Mg) |
150 ppm CaCo3 (3 meq/l) |
|
|
|
|
Factores de salinidad |
|
|
Conductividad eléctrica (EC) para producción general |
0.75 mmho/cm |
|
Sales disueltas totales (TDS) para producción general |
1280 ppm |
|
Radio de absorción de sodio SAR) |
4 |
|
Sodio (Na) |
69 ppm ( 3 meq/l) |
|
Cloro (Cl) |
71 ppm (2 meq/l) |
|
|
|
|
Elementos |
|
|
Nitrógeno total (N) b |
10 ppm ( 0.72 meq/lt) |
|
Nitratos (NO3) |
44 ppm ( 0.72 meq/lt) |
|
Amonio (NH4) |
10 ppm ( 0.56 meq/l) |
|
Fósforo (P) c |
1 ppm ( 0.03 meq/l) |
|
Fosfato (H2PO4) |
3 ppm ( 0.03 meq/l) |
|
Potasio (K) c |
10 ppm ( 0.26 meq/lt) |
|
Calcio (Ca) d |
O a 120 ppm ( 0 a 6 meq/l) |
|
Magnesio (Mg) d |
0 a 24 ppm ( 0 a 2 meq/lt) |
|
Azufre(S) |
20 a 30 ppm ( 0 a 2 meq/l) |
|
Sulfato (SO4) |
60 a 90 ppm ( 1.26 a 1.88 meq / l) |
North Carolina, State University College or Agriculture & Life Sciences
a Aguas con un pH alto se pueden utilizar al neutralizar con ácido los bicarbonatos y otros iones que contribuyen a la alcalinidad.
b El Nitrato y el amonio proveen de nitrógeno a las plantas pero puede indicar que el agua esta siendo contaminada con fertilizantes o con otros contaminantes.
c El Fósforo y potasio normalmente están en concentraciones muy bajas en el agua para riego. Si presenta concentraciones mayores, significa que se puede estar contaminando con fertilizantes o detergentes u otros contaminantes.
d Los límites aceptados de Ca y Mg dependen del balance entre los dos.
La alcalinidad esta relacionad con el pH porque establece la capacidad buffer del agua. La alcalinidad afecta la cantidad de ácido a aplicar para cambiar el pH. Por ejemplo, A) si se cuenta con un agua que tiene un pH de 9.3 y una alcalinidad de 71 ppm de CaCO3, , y se requiere llegar a un pH de 5.8, es necesario aplicar 467 ml de ácido sulfurico del 35 % por 1000 galones de agua. B) Si el agua tiene un pH de 8.3 y una alcalinidad de 310 ppm de CaCO3, y se desea bajar el pH a 5.8, es necesario aplicar 2 litros de ácido sulfúrico al 35% por 1000 galones de agua. Es decir, que en segundo caso es necesario aplicar 4 veces más ácido que en el caso A para bajar el pH a 5.8. En resumen, ambos, pH y alcalinidad son importantes para ajustar el pH del agua.
En el siguiente cuadro se resumen los ácidos comúnmente usados para acidificar el agua de riego y sus propiedades:
|
ACIDO |
Formulación y densidad o w fórmula. (FW) |
Cantidad de ácido a adicionar por cada meq/l de alcalinidad para llegar a 5.8 |
Concentración de nutrientes por cada 30 ml de ácido por 1000 gal agua |
Costo por meq/llt por 1000 gal de agua (Costo 1997) |
Seguridad (relativa) |
|
Acido cítrico H3C6H5O7 |
99.5 % (w:w) granular FW = 192.1 |
9.1 oz/1000 gal |
ninguno |
U$ 0.59 |
Puede causar irritaciones menores en piel y ojos |
|
Acido nítrico HNO3 |
67% (w:w) liquido d = 1.42 |
6.6 fl oz/1000 gal |
1.64 ppm N |
U$ 0.26 |
Usar con extrema precaución. Muy cáustico. No inhalar los gases.. |
|
Acido fosfórico H3PO4 |
75%(w:w) liquido d = 1.58 |
8.1 fl oz/1000 gal |
2.88 ppm P |
U$ 0.44 |
Ligeramente cáustico; puede causar irritación en piel y ojos |
|
Acido sulfúrico H2SO4 |
35 % (w:w) liquido d = 1.26 |
11.0 fl oz/1000 gal. |
1.14 ppm S |
U$ 0.16 |
Ligeramente cáustico; puede causar irritación en piel y ojos |
Alkalinity control for irrigation water used in nurseries and greenhouses. North Carolina State University College or Agriculture & Life Sciences.
El exceso de alcalinidad en el agua de riego, se puede corregir con ácido, siguiendo la tabla siguiente:
Cantidad de ácido (fl oz) por 100 galones de agua para Neutralizar ___________ ppm de CaCo3.
|
ppm CaCO3 a neutralizar |
Acido sulfúrico 93% |
Acido sulfúrico del 33 % |
Acido fosfórico del 85 % |
Acido fosfórico del 75 % |
Acido nitrico del 61 % |
|
10 |
0.074 |
0.210 |
0.175 |
0.212 |
0.312 |
|
25 |
0.186 |
0.524 |
0.437 |
0.530 |
0.780 |
|
50 |
0.372 |
1.048 |
0.874 |
1.060 |
1.560 |
|
75 |
0.558 |
1.572 |
1.311 |
1.590 |
2.340 |
|
100 |
0.744 |
2.096 |
1.748 |
2.120 |
3.120 |
|
125 |
0.930 |
2.620 |
2.185 |
**** |
3.900 |
|
150 |
1.116 |
3.144 |
**** |
**** |
4.680 |
|
175 |
1.302 |
3.668 |
**** |
**** |
5.460 |
|
200 |
1.488 |
4.192 |
**** |
**** |
6.240 |
|
225 |
1.674 |
4.716 |
**** |
**** |
7.020 |
|
250 |
1.860 |
5.240 |
**** |
**** |
7.800 |
Ajuste del exceso de alcalinidad con el uso de ácido en la inyección. North Carolina State University College of Agriculture & Life Sciences.
**** El ácido fosfórico es relativamente ineficiente en esto valores altos
En la selección del ácido es importante tener en cuenta también el costo. Los ácidos nítrico y el sulfúrico son más económicos que el ácido fosfórico.
La fertilización de las plantas madres estará enfocada a la producción permanente de esquejes es decir estará continuamente en estado vegetativo; por tal motivo los niveles de nitrógeno siempre estarán más altos con respecto a las plantas en producción de flor.
La disponibilidad de los elementos esenciales está dada entre otros parámetros por el pH del medio donde se encuentren las plantas. Este comportamiento es diferente en suelo y en sustrato, es decir, en el caso del fósforo en suelo está más disponible en pH entre 6.5 a 8.0 y en sustrato está más disponible en pH entre 4.0 a 5.5.
Este comportamiento
se puede apreciar en el siguiente gráfico: 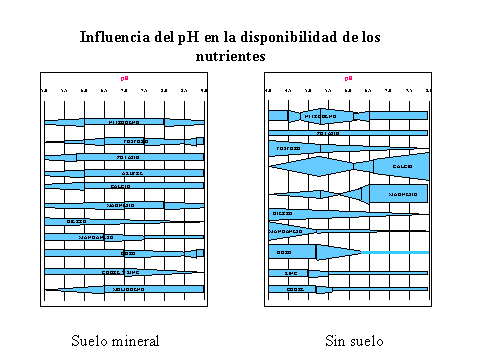
Establecer una recomendación de fertilización para Plantas madres de clavel es difícil, debido a que esta va a depender de factores como el sustrato empleado, pH del medio, la frecuencia de riego, manejo y edad de las plantas madres. Sin embargo, en términos generales, se puede plantear la siguiente fórmula en ppm:
|
N |
P |
K |
Ca |
Mg |
S |
Fe |
Mn |
Cu |
Zn |
B |
Mo |
|
220 |
40 |
180 |
150 |
30 |
20 |
3 |
0.5 |
0.1 |
0.2 |
0.5 |
0.05 |
Para una correcta fertilización , se debe contar con los tanques A y B de manera que en el A se adicionen los fertilizantes a base de Ca y Fe, este de último para no enturbiar la solución desde el comienzo. Al tanque B se le adicionan los que tiene SO4, PO4 y los micorelementos. El resto de los fertilizantes se distribuye en los 2 tanques teniendo en cuenta el equilibrio que debe existir.
Cuando se muestrean sustratos en contenedor, puede ser conveniente desechar la capa superficial de unos pocos centímetros, si se sabe que ha habido una aportación reciente de abonos en superficie. Igualmente, deberá tenerse en cuenta que si se hallan presentes fertilizantes de liberación lenta, la muestra debe ser tomada sin rotura de los gránulos de abono, que deberán ser eliminados, y la interpretación será distinta.
Cuando se sospecha que los problemas de crecimiento son consecuencia de carencias nutricionales, suele resultar útil complementar el análisis químico de sustratos de plantas sanas y afectadas con el análisis foliar de las plantas correspondientes de los mismos contenedores de los que se han tomado las muestras de sustrato. En estos casos es conveniente, aunque resulte mas costoso, analizar por separado varias submuesatas de sustrato y /o planta, para cerciorarse de que las diferencias observadas entre plantas sanas y afectadas no son consecuencia de la heterogeneidad de los materiales.(Ansorena Miner)
PH, CONDUCTIVIDAD Y NUTRIENTES
Los dos primeros parámetros proporcionan una información importantísima sobre el estado nutricional del sustrato, y pueden ser determinados en el cultivo de una manera sencilla, con los pHmetros y conductivímetros de bolsillo.
El contenido en nutrientes ha de determinarse en un laboratorio, La medida del pH y conductividad se efectúa sobre un extracto acuoso del sustrato. Lo que varía de unos métodos a otros es la relación suelo agua, la forma de preparación del extracto y el partir de peso o volumen de sustrato. En este sentido, y dadas las elevada diferencias de densidad de los sustratos, generalmente se parte de volumen, por lo que algunos autores no aconsejan, por ejemplo, aplicar a sustratos la prueba previa 1:5 (p;v) de salinidad de suelos.
BIBLIOGRAFIA
ANSORENA, M. Javier, 1994. Sustratos. Ediciones Mundi-prensa. Madrid .
CHEEVER, David. Ediciones Hortitecnia. 2001.
HARTMAN, H, KESTER. D. propagación de plantas. C.E.C.S.A México 1972
RESH, H.M. 1992. 3 ª edición. Cultivos hidropónicos. Ediciones Mundi-prensa, Madrid.
International Plug Conference. Grower Talks. 1998. Orlando. Water Considerations for Container Production of plants.
Plantaflor. Cultivo y Comercio. Cultivo de rosas en fibra de coco.1999. Pag, 62
Plantaflor. Cultivo y Comercio. Sacos de substrato para el cultivo del clavel. Pag, 76-77
STYER, R. Flora Culture International.Plugs . Europes plug seedling industry. Pag, 16-19
PUUSTJARVI, V.. La turba y su manejo en horticultura. Ediciones de Horticultura. 1994
CALDEVILLA. M.E , LOZANO, G.M. Cultivos sin suelo. Hortalizas en clima mediterráneo. Ediciones de Horticultura. 1993.
CORNELL CORPORATION, www.cals.cornell.edu/dept/flori/grown